當新型冠狀病毒(SARS-CoV-2)肺炎(COVID-19)疫情最初在全球蔓延之時,幾乎所有人都期待著疫苗和藥物盡快問世,從而終結這場疫情。然而,隨著病毒的不斷變異,具有更高傳染性或更致命的突變毒株層出不窮,這場抗疫遠未達到終點。
根據美國疾病控制與預防中心 (CDC) 內部報告,Delta突變株基礎傳染值(R0)達5-9.5,遠超過原始毒株1.5-3.5的數值,傳播速度與水痘相當。與此同時,疫苗也難以阻擋病毒的腳步,1.62 億接種了疫苗的美國人中每周約有 35,000 例有癥狀的突破性感染,疫苗接種者感染Delta毒株的風險僅比未接種者降低3倍。
體液免疫和細胞免疫是人體對抗外來病毒入侵的兩條重要防線,也是新冠疫苗起作用的兩條重要途徑。其中體液免疫機制能夠識別和捕捉體液中的病毒并予以消滅;而細胞免疫則是人體的最后一條防線,主要由T細胞來“追殺”第一條防線外的“漏網之魚”。先前的研究表明,大部分的病毒突變是在缺乏體液免疫反應的情況下累積的,而關于細胞免疫在病毒進化方面的作用的研究仍然較少。
近日,俄羅斯Smorodintsev流感研究所及Skoltech大學等處的研究人員共同在預印本平臺《Research Square》發表了一篇題為“ SARS-CoV-2 escape from cytotoxic T cells during long-term COVID-19 ”的文章,通過對一名感染SARS-CoV-2長達318 天的免疫功能低下的癌癥患者的數據進行分析,揭示了病毒突變以逃避細胞免疫的機制。

https://doi.org/10.21203/rs.3.rs-750741/v1
這項報告提到的主人公是一位被診斷為晚期非霍奇金彌漫性大B細胞淋巴瘤的女性患者,于2020年4月17日首次被檢測出SARS-CoV-2陽性,并且感染狀態持續到2021年3月。感染期間,患者曾兩度發展為重癥COVID-19,持續時間分別為3個月和2個月,并且研究人員在這兩個時期從患者6個鼻咽拭子樣本中分離出了活病毒。
對這6個鼻咽拭子樣本的基因測序結果表明,導致這名患者兩度陷入重癥狀態的是同一譜系的毒株。病毒在患者體內不斷變異,最終積累了40 個突變,遠超一般人群中SARS-CoV-2的進化率,說明病毒已經適應了人體環境。這些突變分布在整個病毒基因組中,影響了26個病毒基因中的18個,其中有8個突變發生在刺突(S)蛋白基因上。
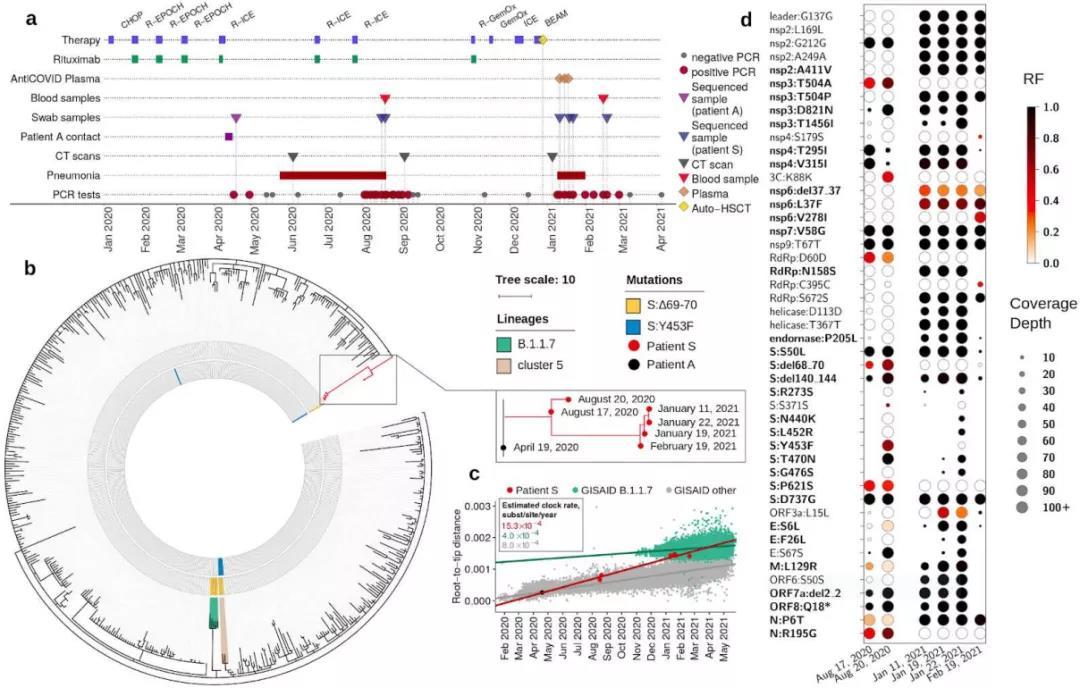
SARS-CoV-2在患者體內不斷進化以適應內部環境
令人疑惑的是,由于這位患者接受了包括利妥昔單抗在內的幾種不同方案下的多個化療周期,這導致患者的體液免疫幾乎“失靈”,既然如此,為何病毒仍然會發生如此多的突變?難道是為了躲避細胞免疫機制嗎?
流式細胞術分析顯示,研究人員確實在患者處于重癥COVID-19期間檢測到了明顯的SARS-CoV-2特異性T細胞反應。而在進一步分析中,研究人員探究了累積的突變是否影響了同種異體抗原HLA的呈遞,結果發現有12 個獲得性突變降低或阻止了HLA I類等位基因的表達,后者為CD8+T細胞的協同刺激分子,表明病毒突變造成了SARS-CoV-2對CD8+ T細胞的免疫逃逸,導致T細胞反應效率低下。
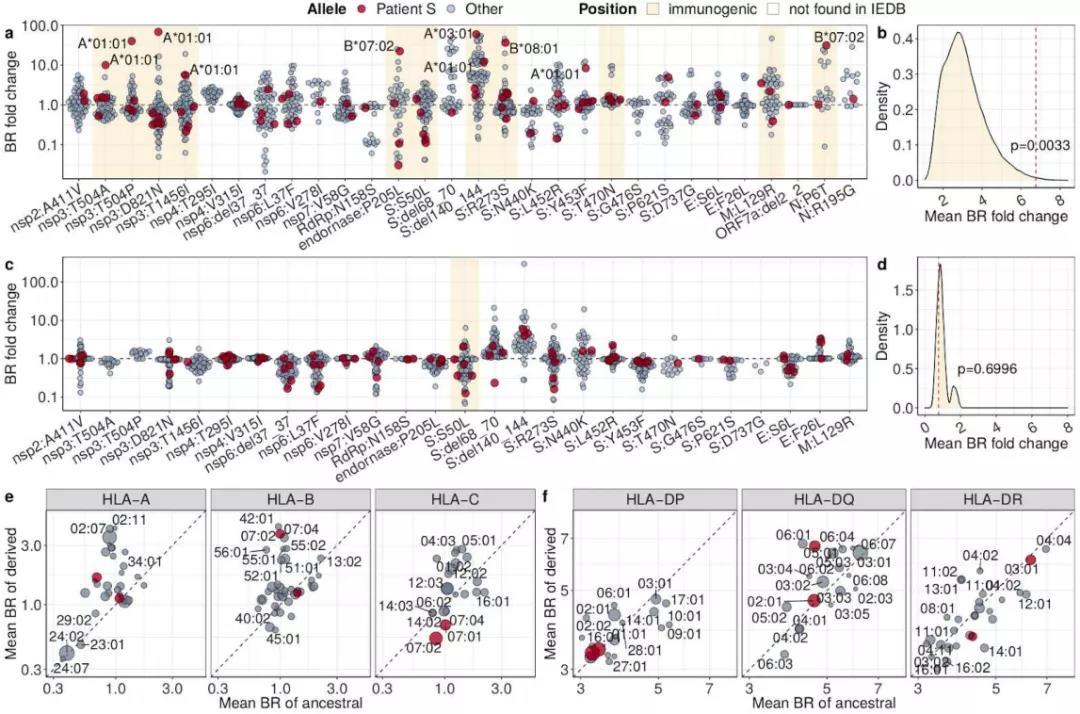
T細胞逃逸突變的群體水平效應
這些結果表明,宿主內進化確實能夠促進SARS-CoV-2對細胞毒性T淋巴細胞的逃逸,這可能是SARS-CoV-2進化過程中一個被低估的因素,應引起重視。
該報告的作者、Skoltech大學的Georgii Bazykin說:“考慮到最近廣泛傳播的SARS-CoV-2變異株,它們的起源可能有些不尋常。當這種變異株開始醞釀時,通常會迅速累積多個突變,就像我們在這項研究中看到的病毒在免疫抑制個體內進化一樣。這可能意味著,一些特殊病例會成為病毒的‘健身房’,使其更好地進化以適應感染人體所需要的體征。盡管我們這項報告中的突變毒株并未流傳出去,但也說明病毒進化的鍛煉場所比我們想象的更具有多樣性。”
End
參考資料:
[1]https://www.researchsquare.com/article/rs-750741/v1
[2]https://medicalxpress.com/news/2021-08-longest-case-covid-sars-cov-immune.html
[3]https://www.livescience.com/internal-cdc-document-covid-delta-variant.html
轉載自|生物探究




 全部商品分類
全部商品分類